iPS細胞を用いた治療薬が保険適用へ|パーキンソン病で再生医療をお受けの患者さんへinformation
iPS細胞を用いた治療薬が保険適用へ
─パーキンソン病で再生医療をお受けの患者さまへ、現時点でお伝えできること
iPS細胞を用いた再生医療等製品が、世界で初めて公的医療保険の対象となりました。日本の再生医療の歴史にとって、節目となる出来事です。
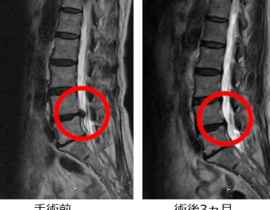
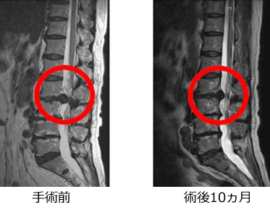
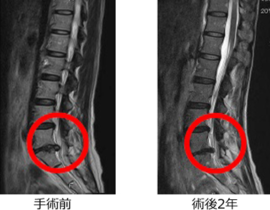
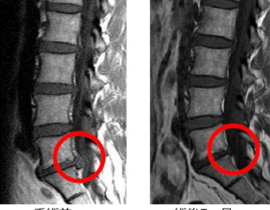
当院では、自家脂肪由来間葉系幹細胞(MSC)を用いた再生医療を、パーキンソン病をはじめとする神経変性疾患の患者さんにもご提供しています。今回のニュースに接して、すでに当院で治療をお受けいただいているパーキンソン病の患者さん、あるいはご家族の中には、「iPS細胞の治療が保険で受けられるようになるのなら、いま受けている幹細胞治療との関係はどうなるのだろうか」と、率直な疑問を抱かれた方もいらっしゃるかもしれません。
この記事は、そうしたご質問にお答えする機会の前に、診療を担当する側の医師として、現時点で正確にお伝えできることを、整理しておこうという趣旨でまとめたものです。
結論を先に述べると、今回のニュースは間違いなくパーキンソン病治療にとって歴史的な一歩ですが、「明日から日本中のパーキンソン病の患者さんが、保険でiPS細胞の治療を受けられるようになる」ということを意味するわけではありません。その理由を、再生医療等製品に特有の「条件及び期限付承認」という制度を踏まえながら、順を追ってご説明します。
事実関係の整理
2026年5月13日、中央社会保険医療協議会(中医協)は、京都大学発の技術をもとに住友ファーマが開発したiPS細胞由来パーキンソン病治療薬「アムシェプリ」について、薬価約5,530万円で公的医療保険を適用することを正式に了承しました。
同治療薬は、健康なドナー由来のiPS細胞からドパミン神経前駆細胞を分化誘導したもので、パーキンソン病患者さんの脳内(被殻)に移植することで、失われたドパミン神経の機能を補うことを目指す治療です。
同じ日には、大阪大学発ベンチャー・クオリプスが開発した、iPS細胞由来心筋シート「リハート」(重症心不全用)も保険適用が了承されました。いずれも、iPS細胞由来の再生医療等製品としては、世界初の事例となります。
2006年の山中伸弥教授によるiPS細胞作製報告から約20年、日本発の基礎研究が、ようやく公的医療保険という「暮らしの近く」に届きはじめました。これは率直に、日本の医療と科学にとっての大きな前進です。パーキンソン病の治療に関わる医療者として、また、当院でこの病気の患者さんをお受けしている立場として、まずはこの一歩を、心から歓迎したいと思います。
「保険適用」と「正式承認」は同じではない
ここからが、もっとも大切なポイントです。
今回の保険適用は、通常の医薬品でいう「正式承認(本承認)」とは異なる枠組みのもとで行われています。アムシェプリが取得しているのは「条件及び期限付承認」と呼ばれる、再生医療等製品に特有の特例的な承認です。
「条件及び期限付承認」とは
この制度は、2014年の薬機法改正によって創設されました。再生医療等製品の特殊性──対象疾患が希少であること、評価指標が多面的であること、患者母集団が限定的であることなど──を踏まえ、従来の医薬品と同じスピード感では実用化が進まないという問題意識から生まれた制度です。
制度の要点をまとめると、次のようになります。
- 一定の安全性が確認されていること
- 有効性が「推定」できる段階に達していること
- 最長7年間に限り、市販を認める
- その期間内に追加のデータを蓄積し、改めて「本承認」を申請する義務がある
つまり、「条件付きで先行リリースし、リアルワールドのデータをもって最終的な可否を判定する」というアプローチです。
アムシェプリの場合の「条件」
アムシェプリについては、住友ファーマに対し、今後7年以内に7施設・計35人の患者さんを対象とした市販後臨床試験の実施が求められています。同日承認されたクオリプスのリハートも、75例の市販後試験データの提出が義務付けられています。
市販後試験の結果次第では、本承認に到達することもあれば、本承認を取得できないこともあり得ます。今回のニュースは、いわばゴールテープを切ったというより、公式記録としての本走がいよいよ始まる、というのが正確な理解です。
過去には「本承認に到達しなかった」例もある
条件及び期限付承認制度の下で承認された製品の中には、残念ながら本承認に至らなかったものもあります。事例を整理しておきます。
- ハートシート(テルモ)
重症心不全治療用の自己骨格筋由来細胞シートとして、2015年9月に条件及び期限付承認を取得。しかし、市販後の検証で当初推定された有効性を十分に示すことができず、2024年7月、厚生労働省薬事審議会は「不承認」と結論し、条件及び期限付承認は失効しました。
- コラテジェン(アンジェス)
慢性動脈閉塞症治療用の遺伝子治療用製品として承認されていましたが、市販後調査で当初の有効性が再現できず、最終的に申請が取り下げられました。承認は失効し、保険収載からも削除されています。
- ステミラック注(ニプロ)
脊髄損傷治療用の自己骨髄由来間葉系幹細胞として、2018年12月に条件及び期限付承認を取得。7年の承認期限満了を控えた2025年11月14日に本承認申請が行われ、現在、厚生労働省にて審査中です。結果はまだ出ていません。
これらは決して、研究者の怠慢や企業の不誠実さによって起きたことではありません。むしろ、世界に先駆けて再生医療の実用化に挑戦した結果として、再生医療というカテゴリーが従来型の医薬品と同じ評価軸では測りきれない難しさを抱えていることが、制度運用を通じて明らかになってきた、と理解すべきものです。
なぜ「本承認」は難しいのか
再生医療等製品が本承認に到達しにくい背景には、いくつかの構造的な理由があります。
対象疾患が希少・難治であること
再生医療の対象となる多くの疾患は、希少疾患や重症難治例です。アムシェプリの場合も、ピーク時の対象患者は年間133人と見込まれていると報じられています。母集団そのものが限られているため、大規模な無作為化比較試験(RCT)を組むこと自体が、倫理的にも実務的にも極めて困難です。
細胞そのものが「製品」であること
再生医療等製品は、化学合成された低分子医薬品とは違い、生きた細胞そのものを製品としています。製造ロットごとの均質性を確保することは、通常の医薬品とは比較にならない難しさを伴います。
評価指標が多面的であること
運動機能、QOL、生活障害度、認知機能、画像所見、バイオマーカーなど、評価軸が多岐にわたります。単一の主要評価項目で勝敗が決まる従来型の臨床試験設計とは、馴染みにくい性質を持っています。
これらの理由から、再生医療は「条件付きで先に出して、リアルワールドでデータを積み上げながら検証していく」というアプローチを、半ば必然的に選ばざるを得ない領域です。これは弱点というより、再生医療という新しい医療パラダイムが背負っている、いわば「宿命」とも言えるものです。
iPS細胞そのものについて──「光」と慎重に語られるべき「影」
ここで、iPS細胞そのものの特性についても、簡潔に整理しておきます。
iPS細胞は、京都大学・山中伸弥教授がノーベル賞を受賞された通り、人類の医療史を書き換える可能性を秘めた革新的な技術です。患者さん自身の皮膚や血液など、あらゆる細胞から作製でき、神経細胞、心筋細胞、網膜細胞など、原理的には人体のあらゆる組織に分化させることができます。この「万能性(多能性)」こそが、iPS細胞の最大の魅力です。
一方で、その万能性の裏返しとして、研究者・臨床家が長く向き合ってきた課題があります。それが「分化制御の難しさ」と、それに付随する「腫瘍化リスク」です。
今回のアムシェプリも、こうしたリスクに対する膨大な品質管理・分化誘導プロセスの最適化を経て、ようやく条件付き承認に到達しています。住友ファーマと京都大学の研究チームが20年近くにわたって積み上げてきた仕事は、本当に称賛されるべきものです。
ただし、それは裏を返すと、「iPS細胞由来の治療を一般化していくためには、それだけ重厚な開発体制と継続的なリスク管理が必要である」ということでもあります。iPS細胞由来の治療が、暮らしの近くで当たり前に選択できる治療になるまでには、相当の時間と、慎重な臨床経験の積み重ねが必要です。
再生医療には「複数のカテゴリー」がある
一般の方にとって「再生医療」と言えばiPS細胞、というイメージが強いかもしれません。しかし実際には、再生医療には複数のカテゴリーがあり、用いられる細胞の種類・由来によって、安全性プロファイルも、現時点での実用化の段階も、大きく異なります。
| カテゴリー | 特徴・性質 | 代表例・現状 |
|---|---|---|
| 多能性幹細胞 (iPS細胞・ES細胞) |
あらゆる組織に分化できる「万能性」を持つ細胞です。可能性は最大ですが、未分化細胞の腫瘍化リスクへの管理が必須であり、製品化には大規模な開発体制が必要です。今回のアムシェプリやリハートが、このカテゴリーの代表例です。 | 今回のアムシェプリやリハートが代表例。今まさに検証段階に入った。 |
| 成体幹細胞 (間葉系幹細胞など) |
成人の体内に存在する幹細胞で、骨髄・脂肪組織・歯髄など、由来する組織によって性質が少し異なります。代表的な間葉系幹細胞は、骨・軟骨・脂肪・筋などの間葉系組織への分化と、組織修復・抗炎症作用に関わるサイトカイン分泌(パラクライン効果)を主たる役割としています。万能性を持たないため、未分化細胞が腫瘍を形成するリスクは原理的に多能性幹細胞より低いとされており、自家(患者さんご自身の細胞)を用いる場合は免疫学的にも安全性が高いとされています。 | 再生医療等安全性確保法の枠組みのもとで、自由診療として臨床現場で広く提供されています。 |
| 体性幹細胞由来の 組織シート・ 遺伝子治療用製品など |
対象組織に特化した細胞シートや、遺伝子治療技術を組み合わせた製品など、多様な形態があります。条件及び期限付承認の対象となっているものも、ここに含まれます。 | 条件及び期限付承認の対象となっているものも含まれる。 |
つまり、「再生医療=iPS細胞」ではありません。それぞれのカテゴリーが、異なる役割と、異なる時間軸を持っています。iPS細胞由来の治療が、これから段階的に検証・普及していくのと並行して、成体幹細胞を用いた治療は、すでに臨床現場で患者さんに提供されているという現実があります。
当院でパーキンソン病の治療を受けておられる患者さんへ
今回のニュースは、繰り返しになりますが、日本の再生医療、そしてパーキンソン病治療にとって、極めて重要な前進です。当院で再生医療をお受けの患者さんにも、ぜひこの進歩を一緒に喜んでいただきたいと願っています。
一方で、再生医療は──iPS細胞由来であれ、成体幹細胞由来であれ──まだまだ発展途上の医療分野です。過剰な期待で受け止めることも、根拠の薄い批判で全否定することも、ともに患者さんの利益にはつながりません。
当院でMSC治療をお受けの患者さんから、今後いただくことが想定されるご質問にも、現時点でわかる範囲でお答えしておきます。
もちろん、個別のご状況によって判断は変わり得ます。ご不明な点、不安に感じておられること、もっと詳しく知りたいことなどがありましたら、ぜひ次回のご来院時に、診察の場で遠慮なくお尋ねください。
おわりに
iPS細胞由来治療の保険適用は、再生医療というカテゴリー全体への追い風です。同時にそれは、再生医療がこれから本格的な検証の時代に入ることを意味します。当院でMSC治療をお受けの患者さんにとっても、再生医療の選択肢が広がっていくことは、長期的には心強い変化のはずです。
当院は、自家脂肪由来間葉系間質細胞(MSC:Mesenchymal Stem / Stromal Cells)を用いた再生医療を、再生医療等安全性確保法の枠組みに準拠して提供しています。この後、続編として、当院がどのような体制・基準でこの医療を実施し、これまでにどのような臨床データを蓄積してきたかについて、特定認定再生医療等委員会への定期報告内容を踏まえてご紹介する予定です。引き続き、ご一読いただければ幸いです。