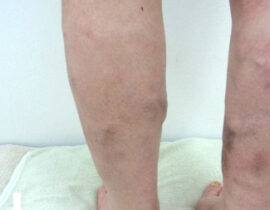
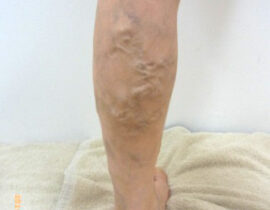
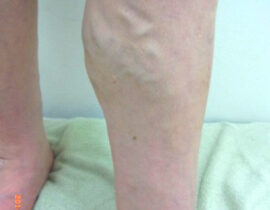
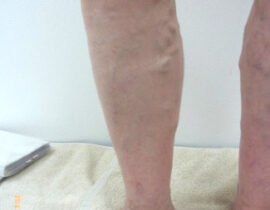
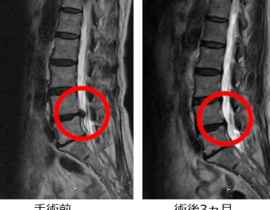
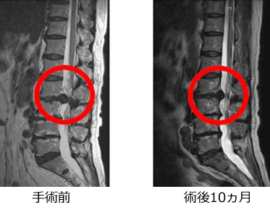
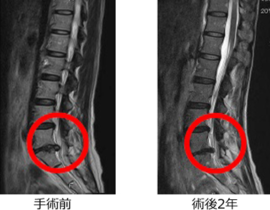
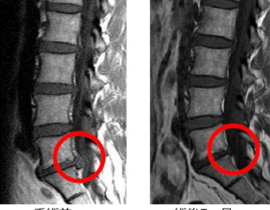
遺伝子治療薬が立て続けに保険収載
近年の遺伝子改変技術の目覚ましい発展により、遺伝子治療は1990年代以降治療対象とされてきた先天性疾患に限らず、がんを含む後天的な疾患など様々な病気の治療選択肢の一つとして注目されています。2019年9月上旬には閉塞性動脈硬化症に対する日本初の遺伝子治療薬「コラテジェン」が保険承認を受け販売が開始されました。当初は、この薬剤を使用して治療が許可される医療機関が相当に限定されますが、新しいタイプの遺伝子治療薬の登場は大変期待されています。また、がん治療においても、再生医療で用いられる細胞の培養増殖の技術と遺伝子導入技術を用いて代表的な免疫細胞であるT細胞を用いた遺伝子治療(CAR-T細胞療法)が、一部の白血病治療薬として本年春にすでに国内で承認されています。手術、放射線、化学療法、免疫療法につぐ、第5のがん治療として遺伝子治療はこれからますます発展していくことが見込まれます。
免疫療法、遺伝子治療が生まれてきた経緯
遺伝子治療は、Ex vivoによるものとIn vivoによるものの二つに分類されますが、それを解説する前に、まず、がんの免疫療法そして遺伝子治療などが生まれてきた経緯に触れたいと思います。そもそも、がん治療は、現在においても手術的治療が最たる根治的治療です。今後、遺伝子治療など先端的治療が発展したとしても、確実に切除できる早期がんに対しては、瞬時にがんを消去できる手術的治療が最も確実な治療法として選択され続けるでしょう。がんが相応に広がってしまってから発見された場合は、体に負担をかけて手術をしても完全に取り除けないため、手術的治療は選択できません。また、発見が早く手術で取り切れる状況であっても、患者さんが体力面で手術に耐えられない場合はそもそも手術が選択できません。そのために、手術以外に、化学療法や放射線治療など他のがん治療が登場してきたわけですが、皆さんご存知のようにこれらの治療法で完全にがんを駆逐するのはほぼ不可能です。これらの治療にも相応の有害事象は避けられません。そのために、有効かつ体への負担が少ない新しい治療として、免疫療法や遺伝子治療が開拓されてきました。免疫療法として活性化リンパ球療法(LAK療法やナチュラルキラー細胞療法(NK療法などが登場した当初は、画期的かつ理想的な治療法として期待されましたが、がんを攻撃する免疫細胞の数が全く不足しており臨床的に抗腫瘍効果が得られませんでした。その後開発された樹状細胞療法なども大量のがん細胞に対して多勢に無勢という印象は拭い去れない状況です。ようやく昨今のオプジーボに代表される免疫チェックポイント阻害剤による治療は、これまでの免疫療法では得られなかった画期的な治療効果を生む例が認められています。ただし、この新しい免疫療法も相応に副作用のリスクがあり、治療適応の制約があることも課題です。直近では、前述の免疫療法と遺伝子治療の技術が融合したCAR-T細胞療法が登場しました。これは一部の白血病に対しては劇的な治療効果を認めます。しかし、やはり相応の副作用があり、薬価が高額で(日本でも1回の治療で3,000万円超)、胃がん、大腸がん、肺がんなどの固形がんには十分な効果がありません。このような状況を背景として、「副作用がなく高い治療効果」を生む理想的な治療法としての遺伝子治療の開拓が今後求められます。
ベクターとは
ところで遺伝子治療においては細胞の核の内部へ遺伝子を導入する必要があります。抗がん剤もその治療機序であるがんDNA合成阻害作用を起こすためには同様に細胞核の中に入る必要があります。ただし、抗がん剤と遺伝子では大きさ(分子量)が全く異なります。抗がん剤はせいぜい分子量500程度ですが、遺伝子は桁違いに大きな分子量になります。すなわち、遺伝子をそのまま細胞にふりかけても、遺伝子は細胞の核の中に入っていけません。つまり、治療に用いる遺伝子をそのまま患部に注射しても細胞核の中には全く入っていません。すなわち、遺伝子治療を行うには治療用の遺伝子を細胞核の中に届けるための運び屋が必要不可欠になります。その運び屋をを「ベクター」と呼びます。ベクターは、ウイルスベクターと非ウイルスベクターの二つに分けられます。ウイルスベクターは原料となるウイルスの感染性を除去して使用されます。また、ウイルスベクターは非ウイルスベクターに比べて遺伝子の導入効率と発現率が大きいのが特徴です。よって、遺伝子治療で用いられるベクターはウイルスベクターが主流です。
Ex vivo 遺伝子治療とIn vivo遺伝子治療
さて、遺伝治療はEx vivo 遺伝子治療とIn vivo遺伝子治療の二つに分けられます。 Ex vivoとはラテン語で「生体外」、In vivoは「生体内」の意味です。すなわち、Ex vivo遺伝子治療は体の外で遺伝子導入する方法、In Vivo遺伝子治療は直接生体内に遺伝子を導入する方法です。先に触れた、CAR-T細胞療法は、患者さんの血液中の免疫細胞(T細胞)を取り出して外部で遺伝子導入することでT細胞を強力にし、さらにそれを培養して増やした後患者さんの体の中に戻す(注射する)治療法で、Ex vivo遺伝子治療に分類されます。一方、In vivo法は、遺伝子製剤を直接患部や生体内に送達して体内で遺伝子発現する方法です。操作が煩雑で極めて高いコストを要するEx vivo法に比べて非常に魅力的ですが、標的となるがん組織に対する遺伝子発現の制御やベクターに対する免疫反応への対処など克服しなければいけない課題があります。 <In vivo 法 と Exvivo法> 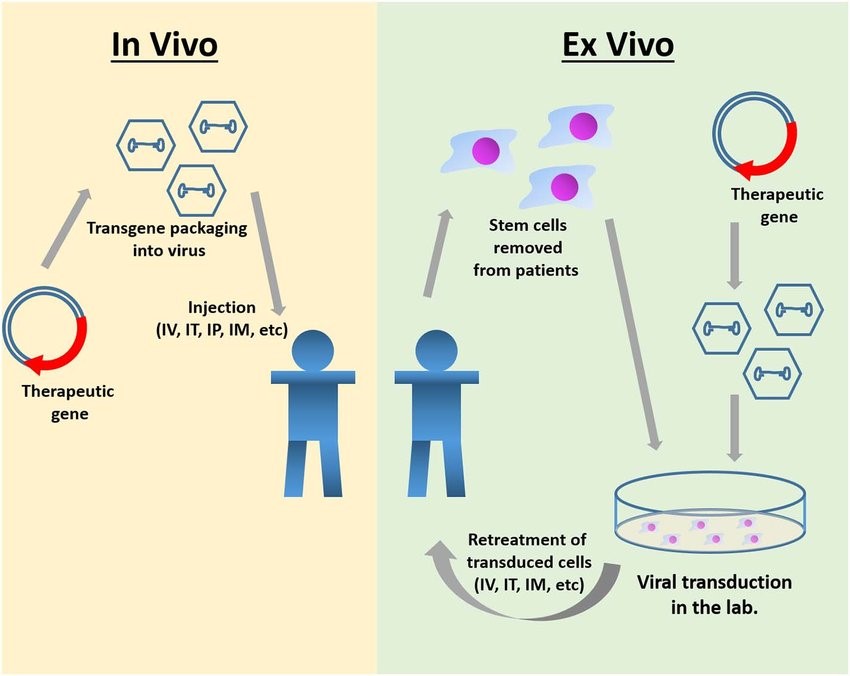
参考:Mol Genet Metab.2018 Feb; 123(2):59-68
CDC6 RNAi 療法への期待
私たちが提供しているがん遺伝子治療CDC6 RNAi 療法は、ベクターとしてレンチウイルスベクターを用いたIn vivo法です。このベクターは遺伝子発現が安定しており、他のベクターに比べて運ぶ容量が大きいため多くの遺伝子を搭載できます。HIVウイルスを由来としている点で当初は不安視する意見もありましたが、ウイルス増殖に必要な遺伝子を欠損させた自己不活性型のベクターであり、機能性と安全面で優れたベクターです。CAR-T細胞療法で用いられたベクターも当初はレトロウイルスでしたが、より強力な新しい世代の療法においてはレンチウイルスベクターが応用されています。レトロウイルスベクターに比べてレンチウイルスベクターは、遺伝子挿入がランダムに分布しやすいことが特徴で、そのためにがん関連遺伝子近傍へのベクター挿入による細胞増殖変化や悪性化を促す変異の発生リスクが低いと考えられています。 また、我々、D.CLINICのCDC6 RNAi 療法では、ベクターにがん細胞に特異的なhTERTを搭載して、がん細胞に取り込まれた時にのみ遺伝子発現が起こるよう工夫されています。 そのため、副作用がほとんどなく寛容性が高いCDC6 RNAi 療法は、画期的ながん治療法として非常に有望視しています。スキルス胃がん、膵臓がん、転移性大腸がん、転移性乳がんなどに対して諦めずに治療に取り組める方法であるだけでなく、今後、リキッドバイオプシーなど、がんの超早期発見技術が整った際には、予防医療の重要なツールとして多くの方に提供できる価値のある治療法として育んでいきたいと考えています。
<A:ベクターの作成 B:電子顕微鏡で撮影されたウイルスベクター>
A: ウイルスベクターを作成するには、レトロウイルス、アデノウイルス、レンチウイルスなどから、感染性や自己増殖性を示す遺伝子領域を除去して、所望の遺伝子発現を来す遺伝子を組み入れる作業が必要になります。 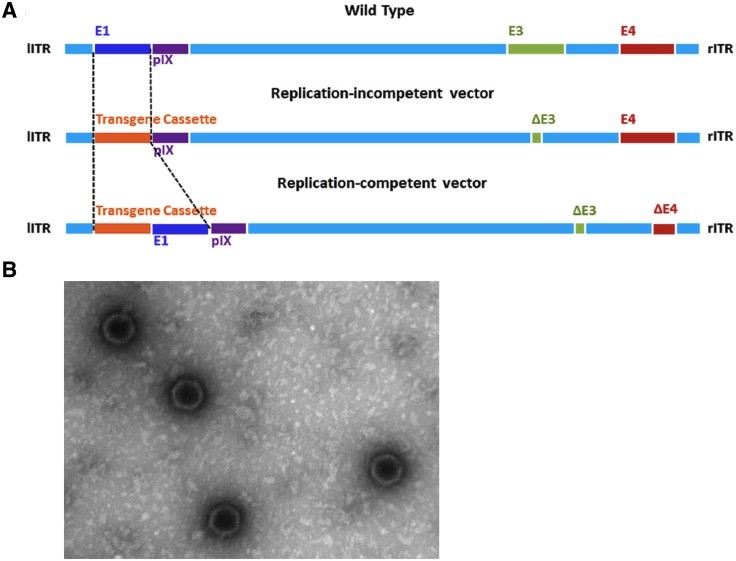
参考:PLoS One 2018; 13(11): e0205139.First-in-human randomized controlled trial of an oral, replicating adenovirus 26 vector vaccine for HIV-1